
雜志:NATURE REVIEWS CANCER
影響因子: 78.5(2022)
年份:2020
通訊作者: Leonard I. Zon
通訊作者單位:Stem Cell Program and Division of Hematology/Oncology, Boston Children’s Hospital and ana-Farber Cancer Institute, Howard Hughes Medical Institute, Harvard Medical School, Boston, MA, USA.
摘要:
在精確腫瘤學(xué)中如筛,有兩種主要策略來預(yù)測臨床相關(guān)腫瘤行為,如治療反應(yīng)和耐藥性的出現(xiàn):基于基因組抒抬、轉(zhuǎn)錄組杨刨、表觀基因組和/或蛋白質(zhì)組分析的推斷,以及個(gè)性化癌癥替身的表型分析瞧剖。后一種方法在歷史上依賴于體內(nèi)小鼠異種移植和體外類器官或2D細(xì)胞培養(yǎng)拭嫁。最近的進(jìn)展在快速組合基因建模,基因免疫缺陷的異種移植在成年斑馬魚和第一個(gè)臨床試驗(yàn)使用異種移植在斑馬魚幼魚表型測試藥物反應(yīng)將這個(gè)微小的脊椎動(dòng)物推到精密醫(yī)學(xué)領(lǐng)域的前沿抓于。在這篇綜述中做粤,我們討論了基于轉(zhuǎn)基因和基于移植的斑馬魚癌癥替身的進(jìn)展,以及這些模型如何與小鼠異種移植和人類類器官進(jìn)行比較和補(bǔ)充捉撮。我們還概述了這些不同的模型為預(yù)測研究提供的獨(dú)特機(jī)會(huì)怕品,以及它們對(duì)未來所面臨的挑戰(zhàn)。
前言
生物醫(yī)學(xué)界一直在開發(fā)越來越多的新型抗癌藥物巾遭。在化療是可獲得的系統(tǒng)性治療的時(shí)代結(jié)束后肉康,一系列新的靶向治療以及免疫治療藥物進(jìn)入了臨床開發(fā)或獲得了監(jiān)管批準(zhǔn)。不斷擴(kuò)大的治療方案為需要系統(tǒng)治療的癌癥患者帶來了新希望灼舍,但也給腫瘤醫(yī)生帶來了新的挑戰(zhàn)吼和。給特定的病人開哪種藥這個(gè)看似簡單的問題越來越難以確定地解決。新藥物的開發(fā)速度超過了需要進(jìn)行的長期和復(fù)雜的試驗(yàn)骑素,以確定哪種劑量炫乓、時(shí)間表和組合策略將為特定的患者群體帶來臨床效益。
精準(zhǔn)腫瘤學(xué)領(lǐng)域誕生于解決這些問題的需要,即創(chuàng)建一種新的預(yù)后和治療范式末捣,專注于對(duì)單個(gè)患者(而非群體)進(jìn)行優(yōu)化治療侠姑。從哲學(xué)上講,精準(zhǔn)醫(yī)療遠(yuǎn)離了基于群體平均水平比較的預(yù)測箩做,而是關(guān)注患者獨(dú)特的疾病特征莽红。
具體來說,在精準(zhǔn)腫瘤學(xué)中邦邦,這種新范式產(chǎn)生了兩種主要方法:其一種方法是基于對(duì)腫瘤活檢樣本的單個(gè)或多個(gè)組學(xué)(基因組學(xué)安吁、轉(zhuǎn)錄組學(xué)、表觀基因組學(xué)和蛋白質(zhì)組學(xué))分析來推斷疾病行為圃酵,由于技術(shù)的改進(jìn)柳畔,這種方法相對(duì)快速且廉價(jià);第二種方法是利用從體外培養(yǎng)或異種移植的腫瘤活檢樣本中獲得的個(gè)性化癌癥替身郭赐,對(duì)腫瘤行為和藥物反應(yīng)進(jìn)行功能測試。作為一種臨床預(yù)測工具确沸,前一種方法受到以下因素的限制:我們對(duì)常見癌癥驅(qū)動(dòng)因素之外的基因中單個(gè)基因突變的功能后果的了解捌锭、事件組合的影響以及克隆動(dòng)力學(xué)和腫瘤進(jìn)化的復(fù)雜性,這些因素可能導(dǎo)致藥物反應(yīng)罗捎。
后一種方法通過模擬聚焦于腫瘤的表型行為和模擬可能的治療設(shè)置來克服這種復(fù)雜性;然而观谦,它受到特定模型的生物學(xué)保真度的限制,作為病人反應(yīng)的代理桨菜,以及后勤方面的考慮——分析時(shí)間豁状、成本和可伸縮性,以及測試多種條件的挑戰(zhàn)倒得。
藥物反應(yīng)的表型測試歷來依賴于在體外培養(yǎng)的患者來源的癌細(xì)胞泻红,如2D培養(yǎng)或3D類器官,或在體內(nèi)培養(yǎng)的小鼠異種移植霞掺。轉(zhuǎn)基因斑馬魚和移植斑馬魚癌癥替身技術(shù)進(jìn)展谊路,加上規(guī)模、成本菩彬、時(shí)間和條件的多重性等內(nèi)在的物流優(yōu)勢缠劝,自動(dòng)化的潛力將斑馬魚帶入精確癌癥治療藥物反應(yīng)的表型測試領(lǐng)域。
在這篇綜述中骗灶,我們重點(diǎn)介紹了工具的歷史和進(jìn)化惨恭,這些工具使得在斑馬魚中快速生成組合轉(zhuǎn)基因癌癥模型成為可能,以及37°C飼養(yǎng)的免疫缺陷斑馬魚的幼魚和成體標(biāo)本異種移植的發(fā)展耙旦。
穩(wěn)定的轉(zhuǎn)基因癌癥模型:
由于與人類廣泛保存器官特異性遺傳程序和癌癥相關(guān)基因脱羡,端粒生物學(xué)上與人類比小鼠更為相似,并且在單細(xì)胞階段通過顯微注射對(duì)胚胎進(jìn)行基因操作相對(duì)容易,斑馬魚很快成為一種有希望在體內(nèi)模擬癌癥的生物體轻黑。

Fig.1 斑馬魚癌癥替身的關(guān)鍵發(fā)展的時(shí)間表糊肤。時(shí)間線強(qiáng)調(diào)了斑馬魚癌癥模型向個(gè)性化患者替身(米色盒子)發(fā)展的關(guān)鍵里程碑。使用小鼠氓鄙、類器官和斑馬魚患者的替身(紫色盒子)預(yù)測癌癥治療反應(yīng)的臨床翻譯中的顯著里程碑馆揉。PDX,患者來源的異種移植物抖拦;zPDX升酣,斑馬魚患者來源的異種移植物。
2003年态罪,首次報(bào)道了斑馬魚T細(xì)胞急性淋巴細(xì)胞白血病(T- ALL)基因工程癌癥模型(圖1)噩茄。將小鼠Myc非保守片段置于斑馬魚rag2啟動(dòng)子的控制下,該啟動(dòng)子限制對(duì)淋巴細(xì)胞的表達(dá)复颈。當(dāng)將其注射到野生型斑馬魚胚胎中時(shí)绩聘,5%的F0斑馬魚在1個(gè)月到5個(gè)月大之間發(fā)育出T-ALL。轉(zhuǎn)基因的種系傳遞使外顯率提高到100%耗啦,降低了腫瘤的潛伏期凿菩。
這個(gè)模型為斑馬魚的癌癥建模提供了一個(gè)顯著的概念證明,并為白血病發(fā)生機(jī)制的新發(fā)現(xiàn)奠定了基礎(chǔ)帜讲。這項(xiàng)研究也為在斑馬魚身上開發(fā)其他腫瘤模型鋪平了道路衅谷,包括2004年的胰腺神經(jīng)內(nèi)分泌腫瘤和2005年的黑色素瘤,從那時(shí)起似将,已經(jīng)建立了許多其他的模型获黔,包括使用Cre介導(dǎo)的重組的條件模型和化學(xué)誘導(dǎo)模型。
然而在验,在大多數(shù)人類癌癥玷氏,特別是實(shí)體腫瘤中,腫瘤發(fā)生被認(rèn)為需要多種基因驅(qū)動(dòng)译红,包括致癌基因的激活和腫瘤抑制因子的缺失预茄。因此,除了RAS驅(qū)動(dòng)的模型外侦厚,僅基于致癌基因表達(dá)的斑馬魚模型普遍表現(xiàn)出較低的外顯率耻陕,這在很大程度上限制了它們的使用。其他局限性包括許多模型是通過一種致癌基因的表達(dá)偶然獲得的刨沦,而這種致癌基因并不總是反映人類腫瘤的早期克隆基因驅(qū)動(dòng)因素诗宣。驅(qū)動(dòng)癌基因表達(dá)的啟動(dòng)子的組織特異性的程度對(duì)于人類腫瘤發(fā)生的忠實(shí)再現(xiàn)也是至關(guān)重要的。
斑馬魚黑色素瘤模型使用了人類黑色素瘤中常見的驅(qū)動(dòng)因子BRAFV600E想诅,放置在黑色素細(xì)胞特異性斑馬魚mitfa啟動(dòng)子的控制下召庞。與人類一樣岛心,BRAF V600E在斑馬魚黑色素細(xì)胞中的表達(dá)只產(chǎn)生豬色素痣。然而篮灼,在斑馬魚體內(nèi)注射攜帶tp53腫瘤抑制基因33失活突變的mitfa:BRAFV600E構(gòu)建體(其人類同源基因在約15%的人類黑色素瘤中發(fā)生突變)在4個(gè)月內(nèi)啟動(dòng)了6%斑馬魚惡性黑色素瘤的形成忘古。這些腫瘤經(jīng)組織學(xué)和表型分析證實(shí)為黑色素瘤。
重要的是诅诱,該病的外顯率在穩(wěn)定期達(dá)到近100%mitfa:BRAF V600E髓堪;tp53?F1轉(zhuǎn)基因斑馬魚。這個(gè)mitfa:BRAF V600E娘荡;tp53?斑馬魚黑色素瘤模型隨后成為多基因篩選的可靠基礎(chǔ)干旁,旨在在體內(nèi)功能性探測人類黑色素瘤遺傳學(xué),并已鑒定出幾種新的黑色素瘤調(diào)節(jié)劑炮沐。雖然這種建模方法非常有價(jià)值争群,但也存在一些技術(shù)上的困難。首先大年,就像其他成熟的轉(zhuǎn)基因斑馬魚癌癥模型一樣换薄,維持含有多個(gè)轉(zhuǎn)基因的穩(wěn)定細(xì)胞系是困難的;其次翔试,可以組合的轉(zhuǎn)基因數(shù)量仍然有限专控,這使得測試復(fù)雜的遺傳相互作用具有挑戰(zhàn)性。第三遏餐,與人類癌基因的過表達(dá)不同,內(nèi)源性斑馬魚腫瘤抑制基因的敲除是系統(tǒng)性的赢底,而不是組織特異性的失都。大多數(shù)模型仍然是基于人類致癌基因的轉(zhuǎn)基因表達(dá),而不是內(nèi)源性或同源斑馬魚位點(diǎn)的敲入幸冻,因此可能沒有生sl理水平的表達(dá)粹庞。基因組編輯技術(shù)的進(jìn)展已經(jīng)并將有助于克服這些限制洽损。
快速組合遺傳建模:
CRISPR–Cas9系統(tǒng)為體內(nèi)癌癥建模創(chuàng)造了新的機(jī)會(huì)庞溜。它允許腫瘤抑制基因的快速鑲嵌失活,繞過穩(wěn)定的轉(zhuǎn)基因系的需要碑定。它還通過靶向不同基因的導(dǎo)向rna(gRNAs)的多重化大大增加了組合建模的潛力流码,使得對(duì)復(fù)雜的人類癌癥基因型的重述和從人類癌癥基因組學(xué)推斷的假定遺傳相互作用的體內(nèi)評(píng)價(jià)成為可能。它促進(jìn)了大規(guī)模的屏幕識(shí)別新的癌癥驅(qū)動(dòng)因素的目標(biāo)延刘。
在老鼠身上漫试,CRISPR使快速建立敲除斑馬魚系成為可能。利用Tol2轉(zhuǎn)座子技術(shù)碘赖,該技術(shù)有助于將DNA結(jié)構(gòu)插入斑馬魚基因組驾荣,CRISPR載體已被開發(fā)用于組織特異性基因失活外构,其方法是將斑馬魚U6啟動(dòng)子驅(qū)動(dòng)的gRNA盒與置于組織限制性斑馬魚啟動(dòng)子控制下的cas9序列組裝在一起。在胚胎組織如肌肉和紅細(xì)胞中觀察到有效的鑲嵌基因敲除播掷。
通過設(shè)計(jì)靶向斑馬魚腫瘤抑制基因的載體审编,并以黑素細(xì)胞特異性的方式表達(dá)人類腫瘤基因,我們能夠通過將BRAF歧匈、NRAS或KIT中的致癌突變與cdkn2a垒酬、tp53、ptena或ptenb中的功能缺失突變相結(jié)合眯亦,快速而有力地模擬人類黑色素瘤中發(fā)現(xiàn)的所有主要基因型(圖2). 侵襲性基因型的腫瘤在注射后3周(NRAS Q61R表達(dá)和tp53缺失)或在幾個(gè)月內(nèi)(BRAF V600E表達(dá)和cdkn2a缺失)就得到了伤溉,這與在人類疾病中的觀察結(jié)果一致。
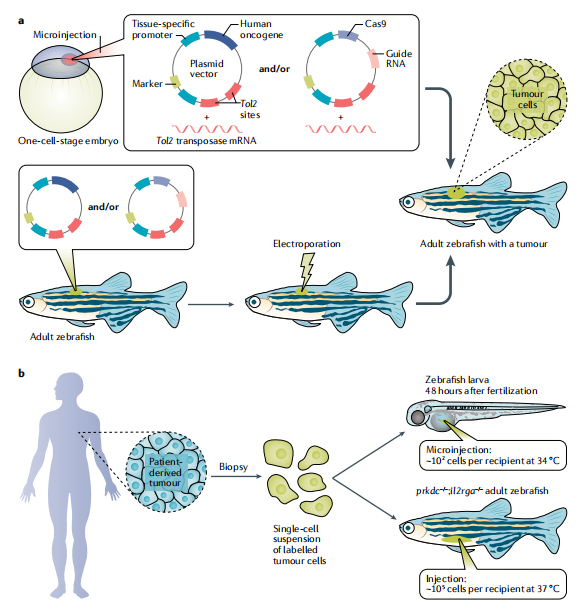
Fig.2 斑馬魚癌癥替身的生成妻率。通過胚胎微注射或電穿孔可以創(chuàng)建|鑲嵌轉(zhuǎn)基因斑馬魚乱顾。在胚胎中(上圖),Tol2 mRNA與含有Tol2位點(diǎn)的質(zhì)粒DNA載體(s)共注射宫静,并被Tol2蛋白識(shí)別并插入宿主細(xì)胞基因組走净。對(duì)于成年斑馬魚的轉(zhuǎn)基因電穿孔,基因傳遞是通過在電穿孔前將表達(dá)Tol2的DNA質(zhì)粒與轉(zhuǎn)基因載體(s)共注射來完成的孤里。在Tol2位點(diǎn)之間伏伯,轉(zhuǎn)基因載體通常包括一個(gè)(1)驅(qū)動(dòng)編碼序列的組織特異性啟動(dòng)子,通常是一個(gè)人類致癌基因12捌袜、23说搅、34、36或Cas9虏等,用于CRISPR敲除腫瘤抑制因子12弄唧、18,以及(2)一個(gè)轉(zhuǎn)基因標(biāo)記霍衫。標(biāo)記通常是由一個(gè)組織啟動(dòng)子和熒光蛋白(例如候引,心臟標(biāo)記cmlc2:EGFP),或者在黑色素瘤的情況下敦跌,一個(gè)微型基因(啟動(dòng)子+編碼序列拯救的損失)澄干,這允許黑素細(xì)胞發(fā)展本身被用作轉(zhuǎn)基因標(biāo)記F0斑馬魚。b|斑馬魚患者來源的異種移植物可以通過移植癌細(xì)胞(通常標(biāo)記)在34°C后48小時(shí)的幼蟲或遺傳免疫缺陷成年斑馬魚(prkdc?/?柠傍;il2rga?/?)°C.斑馬魚胚胎和成蟲保持在26-28.5°C麸俘,而人類細(xì)胞生長在37°C°C.為了支持人類細(xì)胞移植,胚胎在34°C培養(yǎng)(參考13)携兵,這雖然低于人類細(xì)胞的正常生理溫度疾掰,但是斑馬魚胚胎和幼魚耐受的上限。如果溫度從28.5°C緩慢升高到37°C徐紧,每天升高約0.5-1°C静檬,成魚可以忍受在37°C下生活數(shù)月炭懊。
斑馬魚腫瘤異種移植:
斑馬魚作為移植接受者,
斑馬魚有許多固有的特征使它成為理想的移植接受者拂檩。首先侮腹,通過熒光標(biāo)記移植細(xì)胞,可以很容易地追蹤移植的正车纠或惡性細(xì)胞父阻,并且使用光學(xué)透明的casper斑馬魚品系作為受體,可以直接觀察移植物望抽。第二,斑馬魚是高度多產(chǎn)的,成熟的雌性每周能產(chǎn)生數(shù)以百計(jì)的雞蛋,但是很小,所以成千上萬的斑馬魚可以保存在一個(gè)設(shè)施,因此管理和維護(hù)成本相對(duì)較低的老鼠(雖然這可能國家和機(jī)構(gòu)之間的顯著差異,據(jù)報(bào)道,比率是數(shù)量級(jí)的成本約1.05美元每只老鼠和大約0.01美元每成年斑馬魚). 重要的是,可以在執(zhí)行手動(dòng)移植或顯微鏡下注射幾百成年斑馬魚或者幾千斑馬魚魚仔,分別在一天內(nèi)由一個(gè)操作符(圖2 b),促進(jìn)大——規(guī)模和高吞吐量細(xì)胞移植研究與免疫力低下小鼠模型是很難執(zhí)行的加矛。將非免疫匹配的斑馬魚細(xì)胞移植到部分免疫受損的成年斑馬魚體內(nèi)已經(jīng)成為常規(guī)。當(dāng)與斑馬魚模型中可用的大規(guī)模遺傳篩選和藥物發(fā)現(xiàn)平臺(tái)相結(jié)合時(shí)煤篙,這些研究為腫瘤內(nèi)克隆進(jìn)化和異質(zhì)性斟览、治療耐藥、侵襲和轉(zhuǎn)移辑奈、造血和干細(xì)胞移植提供了有價(jià)值的見解苛茂。
斑馬魚幼魚的異種移植:
2006年至2007年,人們首次描述了將人類癌細(xì)胞系異種移植到斑馬魚幼魚中的黑色素瘤鸠窗。此后妓羊,大量研究報(bào)道了將癌細(xì)胞系異種移植到斑馬魚幼魚中。然而稍计,尤其早期的研究并不總是包括對(duì)異種移植存活和增殖的嚴(yán)格評(píng)估躁绸。十年后,三項(xiàng)概念證明研究發(fā)表了臣嚣,它們在斑馬魚幼魚中從血液惡性腫瘤和實(shí)體腫瘤中開發(fā)了患者來源的異種移植(PDXs)涨颜,隨后其他研究顯示了腫瘤細(xì)胞亞群之間的合作,可以協(xié)同促進(jìn)腫瘤進(jìn)展和藥物反應(yīng)的表型測試茧球。
斑馬魚的適應(yīng)性和先天免疫系統(tǒng)在小鼠和人類中高度保守。在斑馬魚中星持,先天免疫在受精后一天開始發(fā)育抢埋,而適應(yīng)性免疫在受精后2-3周左右在形態(tài)和功能上成熟。在早期幼體發(fā)育過程中督暂,免疫缺陷期較短揪垄,這使異種移植的人類或小鼠細(xì)胞移植和短期存活,而不需要對(duì)斑馬魚進(jìn)行免疫逻翁。通過這種方法饥努,多種類型的細(xì)胞被移植到斑馬魚體內(nèi),得到了許多重要的發(fā)現(xiàn)八回,包括控制癌細(xì)胞分化酷愧、增殖和遷移的機(jī)制驾诈,以及治療反應(yīng)。一個(gè)特別的優(yōu)點(diǎn)是野生型斑馬魚幼體在形成色素沉著之前具有天然的光學(xué)清晰度溶浴,這使得移植細(xì)胞的單細(xì)胞分辨率成像乍迄、分析和量化變得容易,這一特性優(yōu)于其他移植模式生物士败。第三闯两,大多數(shù)以幼魚為受體的異種移植實(shí)驗(yàn)是在37℃以下進(jìn)行的,在這些溫度下谅将,移植的人體細(xì)胞不會(huì)以相同的速度增殖漾狼,也不會(huì)形成類似于免疫缺陷的腫瘤塊Nsg小鼠或人類患者。
成年斑馬魚的異種移植:
免疫缺陷斑馬魚模型是開發(fā)的移植異種患者來源的癌細(xì)胞到成年斑馬魚受體饥臂。以前在促進(jìn)異種移植細(xì)胞在成年斑馬魚體內(nèi)的長期移植和存活方面的嘗試包括使用輻射或化學(xué)處理對(duì)動(dòng)物的免疫系統(tǒng)進(jìn)行短暫的消融逊躁。γ輻照野生型或casper受體斑馬魚魚允許穩(wěn)定的移植腫瘤和造血的細(xì)胞移植后20天,因?yàn)橐驗(yàn)檎丈浜?0天宿主免疫系統(tǒng)恢復(fù),但還沒有報(bào)道可能的人類細(xì)胞移植。類固醇藥物地塞米松的長期化學(xué)誘導(dǎo)免疫抑制可使人體腫瘤的一部分移植時(shí)間超過時(shí)間點(diǎn)30天擅笔。由于地塞米松本身是臨床上用于白血病和淋巴瘤的抗癌藥物志衣,這種方法不適合評(píng)估血液和白血病細(xì)胞移植。此外猛们,化學(xué)免疫抑制引入了另一層實(shí)驗(yàn)變異性念脯,并可能導(dǎo)致藥物與被測試劑的相互作用,可能混淆實(shí)驗(yàn)結(jié)果的解釋弯淘,從而阻礙標(biāo)準(zhǔn)化和規(guī)穆痰辏化。
為了克服這些局限性庐橙,Langenau小組建立了一個(gè)成年斑馬魚異種移植模型假勿,該模型允許,通過將prkdc(編碼DNA活化蛋白激酶催化亞單位)和il2rga(編碼白細(xì)胞介素2受體-γa)的純合失活突變導(dǎo)入透明casper斑馬魚體內(nèi)态鳖,實(shí)現(xiàn)人和小鼠細(xì)胞的長期植入和增殖转培。這些有免疫缺陷的斑馬魚是透明的,缺乏T細(xì)胞浆竭、B細(xì)胞和自然殺傷細(xì)胞浸须,并能在37°C存活。值得注意的是邦泄,在37℃飼養(yǎng)斑馬魚沒有發(fā)現(xiàn)任何缺陷删窒,除了增加了飼養(yǎng)的工作量。生存能力高顺囊,斑馬魚對(duì)這種溫度的適應(yīng)時(shí)間很長肌索。
此外,經(jīng)過馴化的斑馬魚在超過28天的時(shí)間內(nèi)成功地移植了大量的人類癌細(xì)胞系和PDX特碳。與幼魚移植試驗(yàn)相比诚亚,成魚移植試驗(yàn)的另一個(gè)主要優(yōu)點(diǎn)是晕换,每只成年斑馬魚可使用的移植細(xì)胞數(shù)量顯著增加(每只斑馬魚可使用200萬個(gè)細(xì)胞),此外亡电,還有實(shí)驗(yàn)窗口較長和人體溫度的優(yōu)點(diǎn)届巩。生長動(dòng)力學(xué)、細(xì)胞增殖和凋亡率與NSG小鼠體內(nèi)相同腫瘤的生長動(dòng)力學(xué)份乒、細(xì)胞增殖和凋亡率相同恕汇。基于在小鼠模型中的經(jīng)驗(yàn)或辖,我們期望prkdc-/- il2rga-/-品系的進(jìn)一步工程可以克服當(dāng)前的限制瘾英,例如,由于魚類和人類細(xì)胞因子之間的有限保守性颂暇,或殘余適應(yīng)性免疫缺谴,并進(jìn)一步提高穩(wěn)定性和增加人類腫瘤的范圍移植。
斑馬魚的藥物測試:
用大量的斑馬魚移植患者的腫瘤或轉(zhuǎn)基因模型可以測試大量的臨床可用藥物耳鸯,由于斑馬魚替身與臨床決策的配對(duì)反應(yīng)可以幫助對(duì)患者進(jìn)行分層湿蛔,以獲得其腫瘤的治療(圖3)。斑馬魚虛擬替身的邏輯優(yōu)勢與其他體內(nèi)特定患者虛擬替身相比县爬,顯著增加了藥物試驗(yàn)的可能規(guī)模(表1)阳啥。

表1 NA,不適用财喳;PDX察迟,患者來源的異種移植;TME耳高,腫瘤微環(huán)境扎瓶。不同國家和畜牧業(yè)規(guī)則和不同機(jī)構(gòu)顯著不同,北美和一些歐洲國家的成本和住房規(guī)則表明畜牧業(yè)物理足跡空間需求(12成年斑馬魚和1成年老鼠~1.2l)113和成本(每3.5l魚缸和美元每老鼠籠泌枪,每只老鼠大約1.05美元和每成年斑馬魚約0.01美元)45斑馬魚至少比老鼠低一個(gè)數(shù)量級(jí)概荷。b藥物篩選吞吐量假設(shè)與臨床決策一致的持續(xù)時(shí)間(天至周):低(1-5化合物)、中(10-50化合物)碌燕、高(~100化合物)乍赫、非常高(~1000化合物)。c此處數(shù)據(jù)基于Yan等人的概念驗(yàn)證研究14陆蟆。需要對(duì)成年斑馬魚PDXs進(jìn)行進(jìn)一步的研究,以概括不同腫瘤類型的移植率惋增、檢測時(shí)間和細(xì)胞數(shù)量叠殷。
斑馬魚的用藥途徑:
斑馬魚的治療方法是將藥物直接加入水中,并將幼魚和成魚浸入水中诈皿。此外林束,成人可以通過腹腔注射給藥或口喂法(圖3)像棘。通過浸沒療法將藥物輸送到幼魚體內(nèi),使得無法準(zhǔn)確評(píng)估藥物劑量壶冒、藥代動(dòng)力學(xué)和藥效學(xué)(圖3)缕题。

Fig. 3|對(duì)斑馬魚的給藥情況。|浸泡在水中和藥物溶液中用于治療斑馬魚幼蟲患者來源的異種移植物(zPDXs)(24孔板中每孔10-20個(gè)受精后24小時(shí)胚胎或每96孔板一個(gè)胚胎)或成蟲胚胎(10厘米培養(yǎng)皿中兩個(gè)成蟲)胖腾。Fior等(5-氟尿嘧啶治療幼蟲)和Ablain等(用BRAF抑制劑達(dá)布拉非尼治療成人)使用了所示的示例化合物烟零。b|口服灌胃也可用于治療成人替身(鑲嵌轉(zhuǎn)基因斑馬魚或zPDXs)。斑馬魚通過使用MS-222單獨(dú)使用或與異氟烷聯(lián)合使用進(jìn)行麻醉和固定化咸作。使用帶有柔性管的注射器灌胃可以分配~3μl藥物溶液(Dang等79描述)锨阿。c|腹腔注射是治療成人替身(鑲嵌轉(zhuǎn)基因斑馬魚或zPDXs)的另一種替代方法。斑馬魚用MS-222或MS-222和異氟烷進(jìn)行麻醉和固定化记罚。自由注射采用10μl容量的注射器墅诡,輸送高達(dá)5μl的藥物溶液。大約3-5個(gè)μl是報(bào)告的可容忍范圍桐智。
相比之下末早,通過口服管飼或腹腔注射給藥的臨床相關(guān)藥物給藥可以更嚴(yán)格地控制給藥,也可以使用混合血漿樣品通過質(zhì)譜法評(píng)估藥代動(dòng)力學(xué)说庭。此外然磷,與浸沒不同的是,灌胃和腹腔注射可以有效輸送水溶性較低的小分子和抗體口渔。人類样屠、小鼠和斑馬魚之間的藥代動(dòng)力學(xué)差異是該領(lǐng)域一直面臨的一個(gè)重要問題,但實(shí)證測試已被有效地用于確定口服灌胃和藥浴治療的劑量轉(zhuǎn)換因子缺脉。
此外痪欲,口服化療藥物(替莫唑胺)和靶向治療(奧拉帕尼)對(duì)成年斑馬魚PDXs (zPDXs)產(chǎn)生的血液藥代動(dòng)力學(xué)特征與人類和小鼠非常相似。因此攻礼,雖然在每個(gè)病例的基礎(chǔ)上優(yōu)化藥物劑量是必要的业踢,但有可靠的證據(jù)表明,藥物動(dòng)力學(xué)本身并不是斑馬魚替身的跨物種障礙礁扮。
臨床反應(yīng)測定:
患者對(duì)癌癥治療的臨床反應(yīng)是通過測量磁共振成像或計(jì)算機(jī)斷層掃描的成像數(shù)據(jù)的腫瘤直徑變化來確定的知举。根據(jù)大小變化,根據(jù)reCisT標(biāo)準(zhǔn)對(duì)患者的反應(yīng)進(jìn)行分類太伊。在小鼠異種移植腫瘤中雇锡,卡尺,計(jì)算機(jī)斷層掃描或正電子發(fā)射斷層掃描僚焦,或熒光素酶生物發(fā)光通常用于腫瘤反應(yīng)測量锰提。
在斑馬魚中,藥物反應(yīng)通過幾種方式進(jìn)行測量:(1)在未標(biāo)記腫瘤細(xì)胞的透明受體中直接成像(特別是對(duì)于作為黑色素瘤的天然豬腫瘤),(2)腫瘤大小的熒光成像(通過用熒光蛋白病毒載體轉(zhuǎn)導(dǎo)患者來源的細(xì)胞(例如立肘,增強(qiáng)GFP)边坤,或用FUCCI4顯示細(xì)胞周期相,(3)通過將癌細(xì)胞暴露于活性熒光染料谅年,或(4)非侵入性地使用超聲波茧痒。細(xì)胞數(shù)(幼魚zPDX)和腫瘤表面積(幼魚和成魚zPDX)已被用作使用RECIST標(biāo)準(zhǔn)的腫瘤反應(yīng)測量。這些方法與斑馬魚平臺(tái)提供的高通量體內(nèi)篩選相結(jié)合融蹂,提供了更快的成像終點(diǎn)旺订,利用實(shí)時(shí)評(píng)估藥物效應(yīng)的能力降低到單細(xì)胞分辨率。
可以測試的藥劑類型:
早期強(qiáng)調(diào)的替身模型和不同生物中的目標(biāo)保護(hù)之間的生物學(xué)差異殿较,直接影響了哪種治療藥物可以被有效評(píng)估(如文中表1)耸峭。許多抗癌藥物已成功應(yīng)用于斑馬魚,包括各種類型的化療淋纲,小分子抑制劑如達(dá)沙替尼和抗體療法如貝伐珠單抗和西妥昔單抗劳闹。例如,成人zPDX模型被用于鑒定多聚(ADP-核糖)聚合酶(PARP)抑制劑olap- arib和化療藥物替莫唑胺聯(lián)合治療橫紋肌肉瘤的有效性洽瞬。聯(lián)合治療的療效在小鼠異種移植模型中得到了再現(xiàn)本涕,進(jìn)一步證明了兩種受體生物模型在藥物測試中的等效性。
該藥物組合目前正進(jìn)入兒科橫紋肌肉瘤的臨床試驗(yàn)伙窃,并代表了從使用斑馬魚的異種移植臨床前研究開始的聯(lián)合治療的臨床試驗(yàn)菩颖。化療對(duì)斑馬魚和人類的靶點(diǎn)具有高度的保守性为障,而使用小分子或抗體的靶向治療則高度依賴靶點(diǎn)的結(jié)構(gòu)保守性來發(fā)揮作用晦闰。因此,通常只有在異種移植細(xì)胞移植模型中才能有效地評(píng)估癌細(xì)胞的內(nèi)在靶點(diǎn)鳍怨。
另一方面呻右,針對(duì)腫瘤微環(huán)境(TME)的靶向治療將根據(jù)確切的靶點(diǎn)保守性表現(xiàn)出更大程度的可行性。類似的考慮也適用于轉(zhuǎn)基因模型鞋喇,在轉(zhuǎn)基因模型中声滥,我們通常引入人類版本的驅(qū)動(dòng)癌基因,但針對(duì)其他基因或合成致死方法的治療是否成功取決于靶點(diǎn)的保護(hù)侦香。與使用NSG小鼠的移植研究一樣落塑,zPDX模型中缺乏患者特異性免疫腫瘤微環(huán)境和/或協(xié)同進(jìn)化,以及缺乏跨物種靶點(diǎn)保護(hù)(例如罐韩,PD1等免疫檢查點(diǎn)的有限序列保護(hù)憾赁,PDL1和CTLA4)對(duì)在斑馬魚替身中提供一個(gè)有效的代理進(jìn)行評(píng)估提出了挑戰(zhàn)患者對(duì)針對(duì)免疫TME的藥物的反應(yīng)。
另一個(gè)混雜因素散吵,特別是在幼魚是潛在的毒性作用龙考,許多抗癌藥物對(duì)斑馬魚受體幼魚本身膘壶,因?yàn)樗?jīng)歷了一個(gè)快速發(fā)展階段。事實(shí)上洲愤,觀察到的腫瘤縮小也可能是毒性對(duì)受體本身的間接影響的結(jié)果,這將損害其支持癌細(xì)胞生長的能力顷锰。
預(yù)測反應(yīng)和抵抗:
斑馬魚替身對(duì)精確癌癥治療的價(jià)值歸結(jié)為:(1)預(yù)測能力柬赐,(2)實(shí)驗(yàn)規(guī)模和(3)為臨床決策提供信息的分析持續(xù)時(shí)間。因此官紫,值得考慮斑馬魚替身在預(yù)測藥物敏感性和耐藥性方面的益處和局限性肛宋。耐藥性通常分為原發(fā)性或固有性耐藥性(當(dāng)患者對(duì)藥物無反應(yīng)時(shí))和繼發(fā)性或獲得性耐藥性(當(dāng)患者對(duì)藥物敏感時(shí)產(chǎn)生耐藥性)。前者通常由腫瘤顯性克隆或TME的遺傳組成決定束世,而后者則被認(rèn)為是通過達(dá)爾文選擇較小的遺傳抗性的預(yù)先存在的克隆或轉(zhuǎn)錄拉馬克適應(yīng)酝陈,然后對(duì)一個(gè)性狀進(jìn)行遺傳固定而獲得的。
以斑馬魚為例毁涉,在BRAF或KIT驅(qū)動(dòng)的黑色素瘤背景下沉帮,通過spred1失活的快速組合轉(zhuǎn)基因模型,探討了斑馬魚的原代遺傳抗性贫堰。用靶向療法對(duì)成年轉(zhuǎn)基因斑馬魚進(jìn)行浸沒治療穆壕,以治療粘膜黑色素瘤患者,結(jié)果顯示這種普遍的功能喪失遺傳事件導(dǎo)致對(duì)抑制KIT酪氨酸激酶活性的藥物產(chǎn)生耐藥性(如文中圖3)其屏。機(jī)制研究進(jìn)一步表明喇勋,MEK和KIT抑制劑聯(lián)合應(yīng)用的潛在療效。由于藥物暴露時(shí)間短確定主要抗性偎行,幼魚和成蟲ZPDX都是很適合解決這個(gè)問題的模型川背。從腫瘤活檢標(biāo)本中提取的幼魚zPDXs與腫瘤類器官非常相似,在手術(shù)前的新輔助治療中可能特別有用蛤袒,有助于快速選擇有效的化療方案熄云。
另一方面,這樣一個(gè)短期的幼魚移植試驗(yàn)汗盘,每個(gè)受體的細(xì)胞數(shù)量有限皱碘,不太可能是一個(gè)很好的預(yù)測繼發(fā)性耐藥性。這在Fior等人的工作中很明顯隐孽。模擬多克隆腫瘤癌椿,移植前將兩個(gè)等基因細(xì)胞系(含突變KRAS的HCT116細(xì)胞和含野生型KRAS的Hke3細(xì)胞)按1:1混合,每個(gè)細(xì)胞用不同的熒光顏色標(biāo)記菱阵。雖然多克隆腫瘤暴露于葉酸-5-氟尿嘧啶-奧沙利鉑(FOLFOX)化療方案導(dǎo)致腫瘤整體縮小踢俄,但Hke3耐藥克隆的大小沒有改變。
因此晴及,如果沒有不同的顏色標(biāo)記都办,即使一個(gè)非常大的亞克隆沒有反應(yīng),一個(gè)實(shí)際的腫瘤也會(huì)被認(rèn)為是敏感的。我們有理由推測琳钉,較長的時(shí)間窗口和較大數(shù)量的成體zPDXs細(xì)胞將更好地定位這些模型势木,以預(yù)測基于較小的遺傳抗性克隆的擴(kuò)增的二級(jí)抗性機(jī)制,或允許轉(zhuǎn)錄適應(yīng)所需的時(shí)間歌懒。
總的來說啦桌,這些替身準(zhǔn)確建模和預(yù)測抵抗力的能力對(duì)于他們的臨床應(yīng)用至關(guān)重要。
本文章原文Fazio, M., Ablain, J., Chuan, Y. et al. Zebrafish patient avatars in cancer biology and precision cancer therapy. Nat Rev Cancer20, 263–273 (2020).
詳細(xì)網(wǎng)址:https://www.nature.com/articles/s41568-020-0252-3



